���A�C�J��50���N���u30�̉f���i�ŒT��h���̂��h�̍��v
��16�� �E�C���X�ƍۂƊ����ǁ@���Q�O�Q�P�N�Q���Q�V���i�y�j���@
���͎��O�ɏ��ł��A���C�ɂ����ӂ��A�Q���҂ɂ́A�������Ɏ�E���łɂ����͂��������Ď��{���܂����B
��16�� �E�C���X�ƍۂƊ����ǁ@���Q�O�Q�P�N�Q���Q�V���i�y�j���@
���͎��O�ɏ��ł��A���C�ɂ����ӂ��A�Q���҂ɂ́A�������Ɏ�E���łɂ����͂��������Ď��{���܂����B

��c�F
�݂Ȃ���A����ɂ��́B�A�C�J����50���N���ŘA����f��̑�16��ځA�^�C�g���́u�E�C���X�ƍۂƊ����ǁv�ł��B���A�R���i�E�C���X�̊����ǂ̖�肪�傫�Ȗ��ɂȂ��Ă��܂��āA�݂Ȃ���́A�e���r�Łu�E�C���X�v�Ƃ��u�ہv�Ƃ��uRNA�v�Ƃ��u���N�`���v�Ƃ��A�����������t�����ɂ��Ă�����ł��傤�B���{�̍����̊Ԃɂ���قǁA�����������t��������O�ɔ�ь����悤�Ȏ��͂Ȃ������Ǝv���܂��B�@���R�ł͂���܂����A�����������������E�C���X��ۂɊ�������Ƃ������ƁA�a�C�ɂȂ邱�ƁA����͂ǂ������ӂ��ɂ��ċN����̂��A�����m��Ȃ���A�����Ɏ��Â�����A�\�h����̂��A���邢�̓��N�`�����g���̂��A�Ƃ��������Ƃ͂킩��Ȃ����ƂɂȂ�܂��B�����ŁA�����͂���������Ԋ�{�̂Ƃ���Ɍ������Ă��f�������{���p�ӂ��Ă��܂��̂ŁA�����Č������Ǝv���܂��B
�@�����̓Q�X�g�G�L�X�p�[�g�Ƃ��āA�o���F�t�搶�����������Ă��܂��B�鋞��w�Ŗ��Ԋw���U����Ă��܂����A��͂ǂ�����đ̂Ɍ����̂��낤���Ƃ����������Ȃ����Ă�����Ƃł��B�����́A�o���搶�ɂ́u�R���i�E�C���X�v�̓��ʍu�`��p�ӂ��Ă��������Ă܂��̂ŁA�݂Ȃ���A���낢�뎿�₵�Ă���������Ǝv���܂��B
�@�܂��́A����I�ȉf�悩�猩�Ă����܂��傤�B�쑺����A���肢���܂��B
�쑺�F
�A�C�J���̐쑺�ł��B�A�C�J���͍��N53�N�ڂł��B����܂�1000�^�C�g���ȏ�̉f�������Ă��܂������A���̑�������w�n�ŁA���ł������ǂ̉f��͂��Ȃ葽���ł��B�����ǂ��̂��̂Ƃ������A�����̂͊����ǂ̖�̉f��ł��B
�@���A���ꂾ���R���i�E�C���X�Ƃ��A�����ǂ�������Ȃ���A���܂��Ɉ�ʂ̕��ɂƂ��ẮA�ۂ��E�C���X����������ɂȂ��Ă���̂ł͂Ȃ����A���߂čۂƃE�C���X�͂��ꂾ���Ⴄ��A�Ƃ������Ƃ��킩���Ă���������A�����������̂ł͂Ȃ����Ǝv���܂��B�����́A����Ȋϓ_����I�т܂����B
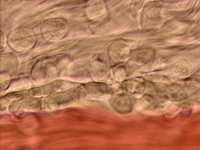
�ŏ��́A�u�k�̊۔��m�̃o�C�I�̖����v�Ƃ����W���̒��̉f���ł��B�k�̊ی����ɉȊw�Z�p�ق�����܂����A���w�҂ő����̂͏��w5�N�����炢�B���̃R�[�i�[�ɁA���ۂ�100���{�̑傫���̍זE�̕��������A�K�ꂽ�q�����~�g�R���h���A�̈֎q�ɍ����Ď����̎���������ނƁA�ǂ�ǂ�g�債�Đ������זE�������ė��āA�f�����n�܂邵�����ł����B�u�a�C�̘b�v�u�ۂƂ̐킢�v�u�C���t���G���U�̘b�v��3�A���3�`4���ł��B�Z���ł����A�����ǂƊ����ǂł͂Ȃ��a�C�A�Ƃ��������̘b���猩�Ă��炦�܂��B
�@���A���ꂾ���R���i�E�C���X�Ƃ��A�����ǂ�������Ȃ���A���܂��Ɉ�ʂ̕��ɂƂ��ẮA�ۂ��E�C���X����������ɂȂ��Ă���̂ł͂Ȃ����A���߂čۂƃE�C���X�͂��ꂾ���Ⴄ��A�Ƃ������Ƃ��킩���Ă���������A�����������̂ł͂Ȃ����Ǝv���܂��B�����́A����Ȋϓ_����I�т܂����B
�ŏ��́A�u�k�̊۔��m�̃o�C�I�̖����v�Ƃ����W���̒��̉f���ł��B�k�̊ی����ɉȊw�Z�p�ق�����܂����A���w�҂ő����̂͏��w5�N�����炢�B���̃R�[�i�[�ɁA���ۂ�100���{�̑傫���̍זE�̕��������A�K�ꂽ�q�����~�g�R���h���A�̈֎q�ɍ����Ď����̎���������ނƁA�ǂ�ǂ�g�債�Đ������זE�������ė��āA�f�����n�܂邵�����ł����B�u�a�C�̘b�v�u�ۂƂ̐킢�v�u�C���t���G���U�̘b�v��3�A���3�`4���ł��B�Z���ł����A�����ǂƊ����ǂł͂Ȃ��a�C�A�Ƃ��������̘b���猩�Ă��炦�܂��B
�� �f�� 2010 �w�a�C�̘b/�ۂƂ̂�������/
�C���t���G���U�̘b�x 11��
��c�F
�ǂ��ł�����? �������킩��₷���ł��ˁB���A�C���[�W���N���Ă��܂��B���������C���[�W�������Ȃ���A������̐��I�ȉf����݂Ă��������Ɨ������₷�����Ǝv���܂��B
�쑺�F
��قǂ̉f��͒��O����̊��ŁA�^�~�t���Ƃ����C���t���G���U�̖������Ă��鐻�[�J�[�ł��B
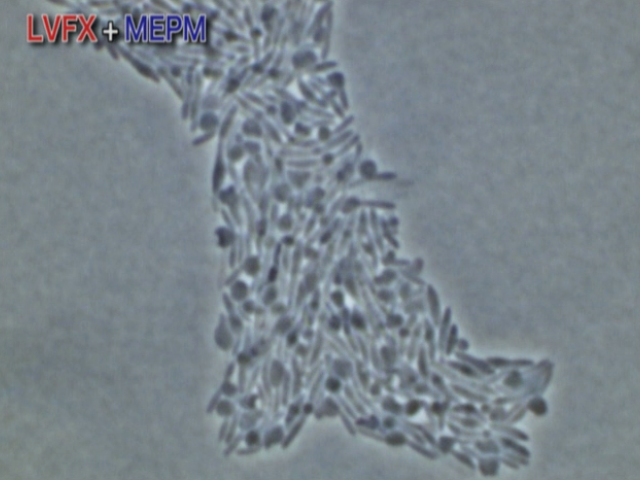
�@���́A���O������̊��ŁA2�̖�܂̕��p���ʂ������ł݂��Ă��܂��B�ďC�͓��M��̊ړc�搶�A�R���i�ЂŃR�����g�����߂��āA�݂Ȃ���������̂悤��TV�ł����q�����Ă���搶�ł��B�����ǂ̂��������������A1��1�^�̖�Ƃ��A1��3�^�̖���܂����A���������ł����ɖ�̌����Z�x�����܂�A�������ɉ������Ă��܂��B��ʂɃO���t���o�Ă��܂����A���̔Z�x�ω��������Ă��܂��B����L���Z�x�ȉ��ɂȂ�ƁA���ʂ��Ȃ��A�ۂ����ȂȂ��B
�@�x���Ƃ��ċz�튴���ǂ��N�����Δ^�ۂɑ��āA2��ނ̖�܂��o�Ă��܂��B��̓��{�t���L�T�V���Ƃ�����ŁA�ۂ�DNA�̕�����j�Q���āA�ۂ����Q���܂��B������̓����y�l���Ƃ�����ŁA�ۂ̍זE�Ǎ�����j�Q���āA�����Ȃ��ŎE���B�ۂɑ����p�̂��������Ⴄ�A����2��ނ�g�ݍ��킹�邱�ƂŁA�Е������ł͓���ۂɑ��Ă��L���Ƃ������Ƃ������Ă��܂��B
����2�܂̂͂��炫���̈Ⴂ�ŁA�������B�e�ōۂׂ̒�����Ⴄ�̂ŁA�킩��₷���Ǝv���܂��B
�@���́A���O������̊��ŁA2�̖�܂̕��p���ʂ������ł݂��Ă��܂��B�ďC�͓��M��̊ړc�搶�A�R���i�ЂŃR�����g�����߂��āA�݂Ȃ���������̂悤��TV�ł����q�����Ă���搶�ł��B�����ǂ̂��������������A1��1�^�̖�Ƃ��A1��3�^�̖���܂����A���������ł����ɖ�̌����Z�x�����܂�A�������ɉ������Ă��܂��B��ʂɃO���t���o�Ă��܂����A���̔Z�x�ω��������Ă��܂��B����L���Z�x�ȉ��ɂȂ�ƁA���ʂ��Ȃ��A�ۂ����ȂȂ��B
�@�x���Ƃ��ċz�튴���ǂ��N�����Δ^�ۂɑ��āA2��ނ̖�܂��o�Ă��܂��B��̓��{�t���L�T�V���Ƃ�����ŁA�ۂ�DNA�̕�����j�Q���āA�ۂ����Q���܂��B������̓����y�l���Ƃ�����ŁA�ۂ̍זE�Ǎ�����j�Q���āA�����Ȃ��ŎE���B�ۂɑ����p�̂��������Ⴄ�A����2��ނ�g�ݍ��킹�邱�ƂŁA�Е������ł͓���ۂɑ��Ă��L���Ƃ������Ƃ������Ă��܂��B
����2�܂̂͂��炫���̈Ⴂ�ŁA�������B�e�ōۂׂ̒�����Ⴄ�̂ŁA�킩��₷���Ǝv���܂��B
�� �f�� 2012 �w�Δ^�ۂɑ��郌�{�t���L�T�V����
�����y�l���̕��p���ʁx 10��
��c�F
���ɂ��ꂢ�Ȍ��ʂ�������Ă�������f����������ł����ǁA�Y��Ȃ������ɏo���搶�ɕ����Ă��������̂ł����A�����������ܓ��^�A�Ƃ����͓̂�����O�̂悤�ɂ����̂Ȃ̂ł���?
�o���F
�͂��A�悭���܂��B���J�j�Y���̈Ⴄ��܂����p���āA�����̑�����ʂ��˂炤���@�ŁA�Տ��ł��悭����Ă��܂��B
��c�F
����͗����Ƃ��̖ǂ��������J�j�Y�����킩���Ă���ꍇ�E�E
�o���F
�͂��A�킩���Ă���ꍇ�ł��B�����y�l���̕��͍זE�ǂ̍����j�Q�܁A�����āA���{�t���L�T�V���͍ۂ̑��B��j�Q����A�Ƃ��ꂼ�ꃁ�J�j�Y�����Ⴂ�܂��B
���ɂ��ꂢ�Ȍ��ʂŁA����͔[���������܂��ˁB���́A������A�t�@�N�^�[������܂��āA��܂̔Z�x�ł��B�Ⴆ�A���{�t���L�T�V�������������Z�x���Ⴉ������A���^�ʂ��Ⴉ������A����قǂ��ꂢ�Ȍ��ʂɂ͂Ȃ�Ȃ����A�Z�x��������A�����ƌ������ǂ��Ȃ邩������Ȃ��B���^�ʂƌ����Z�x�A�������ʂł̔Z�x�̊W�𖾂炩�ɂ��邱�Ƃł����ƌ��ʓI�Ȏ��Â��ł��邩������܂��A�����ŏЉ�ꂽ���̂͂炵�����ʂł��B
���ɂ��ꂢ�Ȍ��ʂŁA����͔[���������܂��ˁB���́A������A�t�@�N�^�[������܂��āA��܂̔Z�x�ł��B�Ⴆ�A���{�t���L�T�V�������������Z�x���Ⴉ������A���^�ʂ��Ⴉ������A����قǂ��ꂢ�Ȍ��ʂɂ͂Ȃ�Ȃ����A�Z�x��������A�����ƌ������ǂ��Ȃ邩������Ȃ��B���^�ʂƌ����Z�x�A�������ʂł̔Z�x�̊W�𖾂炩�ɂ��邱�Ƃł����ƌ��ʓI�Ȏ��Â��ł��邩������܂��A�����ŏЉ�ꂽ���̂͂炵�����ʂł��B
��c�F
�Ȃ�قǁB
KK�F
��A��낵���ł����B�Е���3�^����Ă��܂���ˁB1��1��ł͂��߂Ȃ̂ł���?

�o���F
����Ȃ̂ł����A���͍R�������ɂ͂������^�C�v�������āA�����Z�x���������������Z�x�ˑ����̖�ƁA������́u���Ԉˑ����v�̖���܂��B�ŏ�����j�~�Z�xMIC (minimum�@inhibitory�@concentration)�Ƃ����̂��o�Ă��܂�����ˁB����ȏ�ɂȂ鎞�Ԃ������قnj������ǂ��Ƃ������̂ƁA�Z�x�����������������ǂ����̂�����܂����A�Z�x�������ƁA���x�͕���p���łĂ��܂��A����Ƃ̃o�����X���l���Ȃ���A���^����K�v������܂��B
KK�F
�����Ȃ�ł��ˁB
��c�F
������ƁA��̂��Ƃ��킩���Ă��܂����ˁB(��) �ł́A3�{�ڂɂ����܂��傤���B
�쑺�F
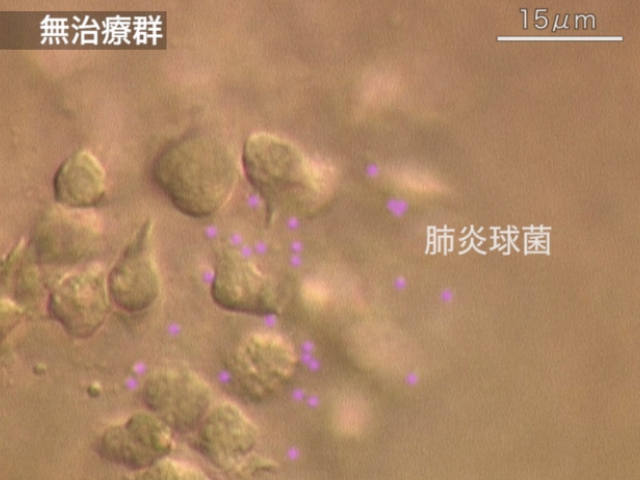
���̉f��́A�ۂɑ��钼�ڂ̖�̌��ʂ��݂����̂ł����B���̉f��́A�̓��ł̖�̂͂��炫�����Ă��܂��B�ŏ��ɁA�C���t���G���U�͂ǂ������a�C���Ƃ����f�悪����܂������A�C���t���G���U�E�C���X�̊����ł��ˁB���̃E�C���X�������N��������ɋN���ė���x���A�I�ɍې��̊������N����₷���Ȃ�܂��B�ۂƖ�̊W�����łȂ��A���ۂɂ͍ۂ͑̂̒��Ŋ������A�̂��������܂��B�ǂ�Ȃ��Ƃ��N���Ă��āA���̎��A��͂ǂ������̂��B
�@�C���͊ǂł����A������\�����Ă���זE�ɂ͋C���̓����ɍׂ����т������āA�ŏ��̉f��Łu�̂ǂ̐��сv�Əo�Ă��܂����B���̐��т��˂˂̔S�t�������āA�C��������Ă��܂��B�����Ȃ��̂������Ă��Ă��A�S�t�ő����āA���тŏ�֏�ւƑ~���o���A�r������Ă���̂ł����A���ꂪ�ǂ��Ȃ��Ă���̂��B
����������A���Ă��������킩��Ǝv���܂����A�������B�e�Ńt�H�[�J�X����̖ʂɍ��킹��A���̖ʂɍ��킹��Ƃ����b���o�Ă��܂��B���̎��A�ǂ������Ă���̂��������}����ʂ̒��ɂłĂ��܂��B�C���̓����\�ʂ����Ă���̂��A���̉��̑g�D�̒������Ă���̂��A�������������B
�@�C���͊ǂł����A������\�����Ă���זE�ɂ͋C���̓����ɍׂ����т������āA�ŏ��̉f��Łu�̂ǂ̐��сv�Əo�Ă��܂����B���̐��т��˂˂̔S�t�������āA�C��������Ă��܂��B�����Ȃ��̂������Ă��Ă��A�S�t�ő����āA���тŏ�֏�ւƑ~���o���A�r������Ă���̂ł����A���ꂪ�ǂ��Ȃ��Ă���̂��B
����������A���Ă��������킩��Ǝv���܂����A�������B�e�Ńt�H�[�J�X����̖ʂɍ��킹��A���̖ʂɍ��킹��Ƃ����b���o�Ă��܂��B���̎��A�ǂ������Ă���̂��������}����ʂ̒��ɂłĂ��܂��B�C���̓����\�ʂ����Ă���̂��A���̉��̑g�D�̒������Ă���̂��A�������������B
�� �f�� 2011 �w�ċz�튴���ǂ��ς�
�@ �C���t���G���U�����ɑ�������ې������x 11��
��c�F
�����������Ƌ����ł���ˁB��̌��ʂƂ����̂��A�זE���x���Ŗڂ̓�����Ɍ�����ꂽ�����ŁA�����A��Ƃ����̂͂���Ȃӂ��Ɍ����A�Ƃ����̂��ƂĂ��悭�`����Ă���f���ł͂Ȃ��������Ǝv���܂��B�o���搶�A�������ł����B
�o���F
����������͂�����܂���B���炵���Ǝv���܂��B��w�̊w���A����1�N���A2�N���ɂ݂���ƁA����͂����w�K�̃��`�x�[�V���������܂�̂ł͂Ȃ����Ǝv���܂��B
��c�F
����͎B�e�̎��ɂ����낢���J�����������Ǝv���܂����A���낢��t�H�[�J�X��ς��Ă��܂���ˁB

�쑺�F
�s���g�̍����ʂ������ł�����A�ォ�A�����A���قǂ��A�B�e�҂��A�ǂ��ʼn����N�����Ă��邩�A�������Ĉꐶ���������Ă����̂ł����A������ς���ɂ킩��悤�ɁA���̓I�ɃC���[�W���Ă��炤�̂ɂǂ��܂Ƃ߂悤���A���H�v�̂��ǂ���ł����B���̎��ɁA���c��̃A�C�f�A�ŁA���A�ǂ̖ʂ����Ă���̂��A�킩��悤�g�D�̒f�ʐ}���o�������������A���ꂪ�킩��Ȃ��ƊςĂ���l���킩��Ȃ��Ȃ��Ă��܂���ƌ������ƂŁA�g�D�̍\���̃A�j���[�V�����������ĕ\�����܂����B
��c�F
�Ȃ�قǁB����ł͍Ō�̍�i�ł����A�������߂�37���ł��ˁB
�쑺�F
�����̂ƁA��Ҍ����ɍ��ꂽ��i�Ȃ̂ŁA��������Ǝv���邩������܂��A���炩���߁B�ȒP�ɉ�����Ă����܂��B
�@1982�N�A���{�̌o�ϐ����ƂƂ��ɁA�C�O���s�������A�A���H�i�������ς������Ă�������A���̃O���[�o�����̑���̊����ŁA�����Ȑl�╨�̈ړ����L�����āA���炽�ȍې��̉����ǁA�ې��������������܂��悤�ɂȂ��Ă������オ�w�i�ɂ���܂��B
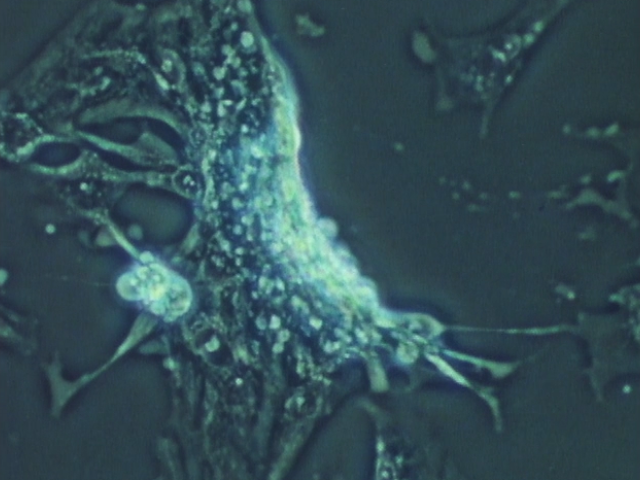
�@����܂ł�3�{�́A�ċz��̊����ǂ̘b�ł������A���x�͌�����H���␅�ƂƂ��ɓ���ۂɂ�钰�̊����ǂ̘b�ł��B�����Ȍ����ۂ��łĂ��܂��B���̍ۂɂ��傫�������ē�A�őf������đ̂����Q������̂ƁA�ۂ��̂��̂��זE�̒��ɓ����đg�D���Ă��܂����̂�����̂ł����A���ꂼ��̓������������Č����Ă��܂��B���ۂɁA�ۂ��זE�̒��ɓ����āA������Ƃ����悤�Ȍ���������܂��̂ŁA��������������Ǝv���܂��B
�@1982�N�A���{�̌o�ϐ����ƂƂ��ɁA�C�O���s�������A�A���H�i�������ς������Ă�������A���̃O���[�o�����̑���̊����ŁA�����Ȑl�╨�̈ړ����L�����āA���炽�ȍې��̉����ǁA�ې��������������܂��悤�ɂȂ��Ă������オ�w�i�ɂ���܂��B
�@����܂ł�3�{�́A�ċz��̊����ǂ̘b�ł������A���x�͌�����H���␅�ƂƂ��ɓ���ۂɂ�钰�̊����ǂ̘b�ł��B�����Ȍ����ۂ��łĂ��܂��B���̍ۂɂ��傫�������ē�A�őf������đ̂����Q������̂ƁA�ۂ��̂��̂��זE�̒��ɓ����đg�D���Ă��܂����̂�����̂ł����A���ꂼ��̓������������Č����Ă��܂��B���ۂɁA�ۂ��זE�̒��ɓ����āA������Ƃ����悤�Ȍ���������܂��̂ŁA��������������Ǝv���܂��B
�� �f�� 1982 �w�ې������@���ǂƎ��Áx 37��
��c�F
�Ō�̉f��́A�܂��ɍ��������������Ă���V�^�R���i�E�C���X�̖��ɂ��Ȃ���e�[�}�������Ă���Ă���̂ł͂Ȃ����Ǝv���܂��B���ƁA�f�������Ƀ��A���ŁA�̂̒��̍זE���A�{���ɓ����Ă���Ƃ������Ƃ��`����Ă���悤�ȁA�f���������Ǝv���܂����A�H���łȂ�āA�������܂�Ȃ���ƈ��Ղɍl���Ă��܂������ł����A���͂����ȒP�ɂ͌����Ȃ��̂ł͂Ȃ����A�Ɖ��߂ē˂������Ă���悤�ȁA�����ȈӖ��ŁA���������w�Ԃׂ����Ƃ̑����f��ł͂Ȃ��������Ǝv���܂��B�o���搶�A�������ł������B
�o���F
����Ƃ��������܂�������ǂ��A��b��������A�Տ������Ɏ���܂ŁA���ꂪ�Љ�₠�邢�͈�Âɗ^����e���܂ł��ׂĂ��܂����ŁA���炵�����e���Ǝv���܂����B����͉��N�ɐ��삳�ꂽ�r�f�I�ł���?
�쑺�F
1982�N�����ł��B
�o���F
30�N�O�ł����B���炵�����Ƃł��ˁB����̃R���i�E�C���X�����ǂ̎Љ���Ɗ֘A���čl����ƁA������x�A�����������Ƃ��l���邫�������ɂ��Ȃ�̂ł͂Ȃ����Ǝv���܂��B�������܂����B
��c�F
�{���ɂ����ł��ˁB�݂Ȃ���������Ȋ��z�����������Ǝv���܂��B���̂��ƁA�����x�e���܂��āA�o���搶����R���i�̂��b���f�������Ǝv���܂��B
�V�^�R���i�E�C���X�����ǂ̂��b�@�o���F�t�搶�@
��c�F
�o���搶�A��낵�����肢���܂��B

�o���F
���߂܂��āA�鋞��w��w���̏o���F�t�Ƃ����܂��B���ً̋}���Ԑ錾�̒��ŁA�����ɏW�܂��ĕ������Ƃ������Ƃ́A�{���ɑf���炵�����Ƃ��Ǝv���܂��B������v���[������X���C�h�́A�鋞��w�̎s���u���Ŏg�������̂ł����A��������k���āA15���قǂ̓��e�ł��b�������Ǝv���܂��B���܂��A����́A�V�^�R���i�E�C���X�ł��ˁB�݂Ȃ���ACOVID-19�Ƃ��ASARS-CoV2�Ƃ����������Ƃ�����Ǝv���܂����ACOVID-19(�R�[�r�b�g�E�i�C���e�B�[��)�͏Ǐ�A�a�C�̖��O�ł����āA�E�C���X�̖��O�́ASARS-CoV2(�T�[�Y�R�u2)�ƌĂ�܂��B���̃E�C���X�Ɋ��������̂�COVID-19�ACorona Virus Infection Disease(�R���i�E�C���X������)�ł��B19��2019�N�ɏo�������Ƃ������Ƃł����܂����B
�@����͐���̉f��ł��o�Ă����C���̐��тł��B���̐��тɂ܂Ƃ����悤�ȁA�ԐF�ɐ��߂Ă���̂�(�d�q�������Ō���)�R���i�E�C���X�ł��B�Ռ��I�Ȏʐ^�ł��B
���u�R���i�E�C���X�̌`�v�ł��B�d�q�������ʐ^�Ɩ͎��I�Ȑ}�ł��B�R���i�E�C���X�͒��ɂ��̂悤��m-RNA(���b�Z���W���[RNA)�̈�`�q���܂܂�Ă��܂��B1�{��RNA�ł��B�j�_������̂悤�Ɍq�������`�����Ă��܂��B���̎������芪���Ă���̂��������ł��B�G���x���[�v�Ƃ����܂��B�����āA���̊ԂɁA�^���p�N�������܂����悤�Ȍ`�ɂȂ��Ă��܂��B���̌`�������Ɏ��Ă��邱�Ƃ���A�R���i�ƌĂ�Ă��܂��B���́A���̃^���p�N���������������ł���B���ꎩ�g�ɂ͑��B�@�\�͂���܂���B���ꂪ�������邱�Ƃɂ���āA���B�����ł��B������ł���ˁB�Ȃ��A����Ȃ��Ƃ����R�E�ɑ��݂���̂��B�܂��܂��s�v�c�Ȃ��Ƃ��������邩�Ǝv���܂��B
�������āA���������E���ɍL����܂����B�R���i�E�C���X�����ł͊����͊g�債�Ȃ���ł��ˁB�Ȃ����Ƃ����A�l���}�̂ƂȂ��Ċ������g�傳�����̂ł��B�̂Ȃ炱��ȂɃp���f�~�b�N�ɂȂ�Ȃ���ł��ˁB�q�H�ƊC�H�����B�������߂ɐl�����R�ɍs�����ł���悤�ɂȂ�܂����B���������ӂ��ɂ��āA�S���E�Ɋg�債�Ă��܂����Ƃ������Ƃł��B
���u�V�^�R���i�E�C���X�����ǂ̏Ǐ�Ɛi�s�v�ł��B���J�Ȃ̃z�[���y�[�W�ɂ����悪�o�Ă��܂��B�܂��A���ǂ����1�T�Ԓ��x�A8���̊��҂͌y�ǂ̂܂������܂��B���̎��́A���M�⊣�����P�A�ؓ��ɂȂƁA��ʓI�ȕ��ׂ̏ǏN����܂��B�����āA�����I�Ȃ��Ƃ́A�����ɏ����Ă��܂��A�������ُ�ɂȂ��ł��ˁB���X�`�̓��������Ȃ��A�J���[�̖������Ȃ��B�����������̖������������ȁA�Ƃ������Ƃ��N����܂��B
�@�����āA�����҂�20%�ŁA�x���Ǐ������A���@�ƂȂ�܂��B��قǂ̉f��ŁA���̍ۊ���������܂������A������݂Ȃ������Ă���Ǝv����ł��B�R���i�E�C���X���������āA�C�����זE������Ă��܂��ƁA�����ɍۂ����荞��ł��܂��B����ɔx�����d�lj����邱�ƂɂȂ�ƁA���̏ꍇ�A�����x�ł��āA���M�∫���A���ꂪ�N����܂��B�F�����TV��V���Ō������Ƃ�����Ǝv���܂����A ��ɂ͂߂Ď_�f�Z�x�𑪂�������܂���ˁB�݂Ȃ���͂ǂ̂��炢�̒l���ł����Ƃ�����܂���?
��c�F
�_�f�Z�x���肳�ꂽ���Ƃ�����܂���?
MS�F
�Ƃő����Ă��܂����A98�Ƃ��B���ɂ����95�Ƃ��B

�o���F
90���炢�ɂȂ�Ɗ�Ȃ���ł���ˁB����98�Ƃ�99�̒l���łĂ��܂��B����ł���ɏd�ǂɂȂ�܂��ƁA�l�H�ċz�킪�K�v�ɂȂ�킯�ł��ˁB��_�f�Ǐ�ɂȂ��ĒE�����N�����܂��BECMO(�G�N��)�Ƃ������O�������Ƃ�����Ǝv���܂��B�C�Ǒ}�����āA�ċz���m�ۂ���킯�ł��B���́A���A�ʂ̕a�C�œ��@�������Ƃ�����܂��B5���ԁA�l�H�ċz���̌����܂����B���̎��ɂ͑S���ӎ����Ȃ���ł��B�Ƃ����̂��A�l�H�ċz������Ă�����A���҂���͖\��܂���ˁB�\�����̂ł�����A���Í܃v���|�z�[���𓊗^������ł��B
�l�͋A�҂��܂������A���́A�����ŖS���Ȃ銳�҂���͈ӎ����Ȃ��܂܁A�S���Ȃ��Ă��܂���ł���B����͉Ƒ��ɂƂ��Ă͗҂������Ƃł���ˁB�݂Ȃ���A�����������Ƃ�m��Ȃ��l��������������܂���B�Ⴂ�l�������������Ƃ�m���Ă�����A���l�Ɋ��������Ă͂����Ȃ��Ƃ����ӎ��ɂ��Ȃ�Ǝv����ł��B
���u�V�^�R���i�E�C���X�̑̓��ł̓����v������������Ǝv���܂��B�̓��ł̓����ƂƂ��ɁA�ǂ��ɂǂ��������������B�����āA�Ō�ɏ������N�`���̂��Ƃ�������܂��傤�B
�@�V�^�R���i�E�C���X�́A�܂��ċz�킩������Ĕx�̐[���ɐN�����܂��B�ʏ�A�C�ǎx�̐��эזE���E�C���X���q��̊O�ɏo����ł����A�������N���čזE���Ă��܂��ƁA�E�C���X�͔x�̐[���܂ŐN�����Ă��܂��܂��B�x�̍זE�ɂ�ACE2��e�̂��������Ă��܂��B�����ɐV�^�R���i�E�C���X���������A��������ƁA�זE�����זv���ăE�C���X�͍זE���ɓ����Ă��܂��܂��B�זE���ł́A�E�j���āi�O���̃G���x���[�v�����āj�A��`�q���o�ė��Ă��܂��B���̈�`�q�̓q�g�̍זE�̗l�X�ȑ��u�ƍޗ����g���đ��B���܂��B�ŏI�I�ɂ́A���̃R���i�E�C���X�̌`�ɂȂ��āA�זE����o�čs���B���̂悤�ȃv���Z�X���J��Ԃ��đ̓��ŃR���i�E�C���X�����B���܂��B
�@���B�����E�C���X�͔x����A���ǂ�ʂ��đ̂̐[���܂ŐN�����܂��B�S�g�ɍs���Ƃǂ��������Ƃ��N���邩�B�Ɖu���������������āA�E�C���X��������悤�Ƃ��܂��B�Ƃ��낪�A���̎��ɁAIL-6 (�C���^�[���C�L��6)���o�ė��܂��B���ꂪ�����I�ɏo�Ă���ƁA�����ȑ���⌌�ǂ̒��Ō������`������܂��B�����ŁA���t�̗��ꂪ�~�܂��āA������s�S���N����悤�ł��B
�������ǂ��N���������ɁA�u�ǂ̂悤�Ȃ��g���Ă��邩�v�ƌ�������E�E���ꂾ���̖g���Ă��܂��B
�@�݂Ȃ���@�u�t�T���v(��ʖ��i�t�@���X�^�b�g)�͕��������Ƃ�����܂����B�܂��L������Ȃ���������܂���B
�A�u�����f�V�r��(��ʖ�)�v�͕��������Ƃ�����܂���ˁB���ꂩ��A�B�u�A�r�K��(��ʖ��t�@�r�s���r��)�v�͕x�m�t�B�����ƕx�R���w�������ō���Ă��܂��B���ꂪ���F�����Ƃ����Ǝv���܂����B
���Ƃ́A�C�u�f�L�T���^�]��(��ʖ�)�v�ƇD�u�I���x�X�R�v(��ʖ��V�N���\�j�h)�͉��ǂ��~�߂�R���ǖ�ŁA���t�玿�X�e���C�h�ł��B
������́A�E�u�A�N�e�����v(��ʖ��g�V���Y�}�u)�A�߃��E�}�`�Ɏg���Ă��邨��ł��B
����炪���Ö�̌��ɂȂ��Ă��܂����A�V�^�R���i�E�C���X�̎��Â̂��߂ɍ��ꂽ����ł͂Ȃ��̂ł���B�Ȃ����Ƃ����A��������ɂ�10�N���炢������B
��������g�����Ƃ���ƁA���łɏ��F����Ă����A������p���Ďg���Ă���̂ł��B

�o���F
�������̖u�ǂ��Ɍ������v�A���������Ȋw�I�ɐ������܂��B�@�܂��A�זE�ւ̐N���Ɍ����̂��A�@�u�t�T���v(�i�t�@���X�^�b�g)�ł��B
�@�����āA�B�u�A�r�K���v�ƇA�u�����f�V�r���v�A����̓E�C���X�̑��B��}���܂��B���ǂ��N���������Ɍ����̂��A�E�u�A�N�e�����v(�g�V���Y�}�u)�ł��B
������ł́A�זE�ւ̐N�������Ă݂܂��傤�B�R���i�E�C���X�͎���Ƀ^���p�N��������ƌ����܂������A�X�p�C�N�^���p�N�ƌĂ�Ă�����̂ł��B���ꂪ�זE���̎�e�́i�M�̕����ł��j�Ɍ������܂��B��������ƁA��e�̂̉��ɂ���^���p�N�����y�f�̓����ɂ���āA�ŏI�I�ɂ̓E�C���X�̖��ƍזE�̖����Z�����āA�E�C���X���זE���ɐN�����܂��i�G���h�T�C�g�[�V�X�ƌ����܂��j�B?�u�t�T���v�́A���̃v���Z�X����p���ăE�C���X�̍זE�ւ̐N����}���邨��ł��B
���B�u�A�r�K���v�͍זE���ł̃E�C���X�̑��B��}���܂��B�E�C���X�̈�`�q�́A�j�_����(A�AU�AG�AC)�����̂悤�Ɍq�������`�ł��B�E�C���X�̒��ɂ���̂́A��{�����Ȃ̂ł��B����ɃA�f�j���Ȃ�`�~���A�O�A�j���Ȃ�E���V���Ƃ�������q�����āA����I�ȍ�������Ă����܂��B���̊j�_���Ȃ��������ARNA�|�������[�[�Ƃ����y�f�ł��B����RNA�|�������[�[�̊������~�߂�̂��u�A�r�K���v�ł��B
���B�u�A�r�K���v�ƇA�u�����f�V�r���v�͓����悤�ȓ��������܂����A���́u�A�r�K���v�͍Ê�`��������܂��B�D�P���Ă��銳�҂���⌋�����Ă��q�����~�����j�����҂���Ƃ��A���̕������ނƁA�D�w�ɉe����^����\��������B���������Ő��������Ƃ������Ƃ����ɂȂ��Ă���悤�ł��B������������A���F����邾�낤�ƌ����Ă��܂��B
���C�u�f�L�T���^�]���v�ƇD�u�V�N���\�j�h�v�͑̓��ʼn��ǂ��~�߂��ł��B�T�C�g�J�C���X�g�[���Ƃ����̂������Ƃ�����Ǝv���܂��B�T�C�g�J�C���̗��A�T�C�g�J�C���̕��傪�\�����錻�ۂł��B�x�̒��ɃE�C���X���N�����āA�����ĖƉu�������N����A�Ɖu�S���זE������������āAIL-6�Ȃǂ̃T�C�g�J�C�������傳��A����ɖƉu�זE������������āA�����זE��������Ă��܂��B�ʏ�͂��������v���Z�X�������܂��B�Ƃ��낪�A�ߏ�ȃT�C�g�J�C�������傳��邱�Ƃ�����܂��B����ɖƉu�זE������������āAIL-6�Ȃǂ����ʂɕ��o�����B���̃T�C�g�J�C������ʂɏo�Ă���B���ꂪ�T�C�g�J�C���X�g�[���ł��B���̂悤�ȏ�ԂɂȂ�Ɛ���זE������Ă��܂��܂��B
IL-6�́A�זE�ɍ�p���鎞��e�̂Ɍ������܂��B���̎�e�̂ւ̌�����j�Q����̂��A�E�u�A�N�e�����v(�g�V���Y�}�u)�ł��B

���ڂ��ė~�����̂́u3�퍬���v�A�A�u�����f�V�r���v�C�u�f�L�T���^�]���v�E�u�A�N�e�����v(�g�V���Y�}�u)��3�퍬�����Ďg���ƌ��I�Ɏ��S�҂����������Ƃ���������܂��B
��łȂ��āA��p�@���̈Ⴄ���g�ݍ��킹��ƁA�����ʓI���Ƃ������ƂȂ�ł��ˁB
��������A�S�z�Ȃ̂��u���ǁv�ł��B���҂�44.%�Ɍ��ǂ��c��ƌ����Ă��܂��B�����̎��̒ቺ���݂��Ă��܂��B���ӊ��A�ċz����A����A���̒ɂ݂�i����l�̊����������Ȃ��Ă��܂��B
�d�v�Ȍ��ǂ�1�Ɂu�u���C���E�t�H�O�v�Ƃ����̂�����܂��B�]�̖��Ƃ������̂ŁA�Ȃ�Ƃ��d�������Ȃ��Ă��邯�ǁA�����v���悤�ɂ͂��炩�Ȃ��A�W���͂��������A�Ƃ����悤�ȏǏN����܂��B����͂ǂ̂悤�ɂ��ċN����̂��B�]�ɂ����ȕ���������Ȃ��悤�ɂ��Ă���]�֖傪����܂��B�Ƃ��낪�A�V�^�R���i�E�C���X�́A���t�]�Ґ��t�֖傩��N������̂ł͂Ȃ����A�Ƃ��������҂����܂��B������A�l�̉����ł����A�@�͕@�S������傫�ȕ��q��]�Ɏ�荞�ދ@�\�������ł���B�V�^�R���i�E�C���X�́A�@���犴�����₷���ł���ˁB�@�o������]���ɍs���Ă��܂����[�g������̂ł͂Ȃ����B�l�͂��������𗧂ĂĂ��܂��B���������ӂ��ɂ��ĐV�^�R���i�E�C���X���]�ɓ��邱�ƂŃu���C���t�H�b�O���N����̂ł͂Ȃ����ƁB
�����Ƃ͂����Ȃ�����܂��āA�u���a�R�́v�B�V�^�R���i�E�C���X�𒆘a����悤�ȍR�́A����̗Տ��������i�߂��Ă��܂��B
���Ō�́u���N�`���v�ł��B�݂Ȃ���̓C���t���G���U�̃��N�`����ł������Ƃ�����܂���ˁB���N�`���̒�`�́A�����ǂ�\�h���邽�߂ɗp����\�h�Ȃ�ł��B�a���̂�����ꂽ���̂��A��ʼn����ꂽ�R���𓊗^���邱�ƂŁA�g�̖̂Ɖu���������āA�����ɔ�����Ƃ������̂ł��B
���̃��N�`���ɂ͂����Ȏ�ނ�����܂����A�t�@�C�U�[�̃��N�`���́Am-RNA(���b�Z���W���[RNA)���N�`���A����͐V�^�R���i�E�C���X�̃^���p�N���ɂ�������̂�̓��ō���悤�Ȉ�`�q���܂܂�Ă��郏�N�`���ł��B���^����ƁA���R�Ɖu�Ɠ����悤�ɑ̂̒��ōR�̂������B��������ƁA�V�^�R���i�E�C���X�������Ă��Ă��A��������������B�����������Ƃ��ł��郏�N�`���ł��B
�@���́A�݂Ȃ���A�}�X�N����Ă��܂��ˁB��������R�Ɖu�̈���ƌ����Ă��܂��B�Ȃ����Ƃ����A�}�X�N���邱�ƂŃR���i�E�C���X�͑�ʂɑ̓��ɓ����Ă���Ȃ����ǁA�킸���ɓ����Ă��Ă���\��������B����ɂ���čR�̂��ł��Ă���B������A���ʓI���Ƃ�������������܂��B
����������A�A�X�g���[�l�J�̃��N�`���B����͂܂��^�C�v���Ⴄ�B�E�C���X�x�N�^�[���g�������̂ł��BS-�^���p�N�A�X�p�C�N�^���p�N����������悤�Ȉ�`�q�����������̂ł��B
�t�@�C�U�[��m-RNA�̃��N�`���ƁA�A�X�g���[�l�J�̃��N�`�������A�嗬�ɂȂ��Ă��܂����A���ɂ������Ȏ�ނ̃��N�`�����n���Ă��܂��B���{�ł́A���O���B�V�I�m�M��������Ă��܂��B���������œ��{���̂��̂��ł���A�����ƌ����I�ɂ݂Ȃ���ɓ��^�ł���悤�ɂȂ邩�Ǝv���܂��B
�����łɈ�Ï]���҂͑łĂ܂���ˁB���́A����̏ꍇ�A���ˍ܂̒�����鋞��w����낤�Ƃ��Ă��܂��B�����ŁA��w���̉�X�E������`���\��ɂȂ��Ă��܂��B�Љ�ɍv�����Ă���܂��B���N�`���͕��������|���ƌ����������������Ⴂ�܂�����ǂ��A�C���t���G���U���N�`�������p�[�Z���g���̊����ŃA�����M�[�╛�������N����܂��B���N�`���Ŋ�����\�h���邱�Ƃ͑�Ȏ����Ǝv���܂��̂ŁA���N�`�����邱�Ƃ����͂����߂��܂��B�@�ȏ�ł��B
��c�F
���̂��b���āA�搶�Ɏ��₵�������Ƃ��o�Ă������Ǝv���܂��B�ǂȂ����A�������ł����B

KK�F
���肪�Ƃ��������܂����B�搶�̂��b�ŁA�R���i�E�C���X�̍זE�ւ̐N���E���B�E���ꂩ��o�čs���Ƃ���ł����A�C���t���G���U�E�C���X���C���[�W���Ă���̂ł����A�E�C���X���זE����o�čs���Ƃ���͗e�ՂȂ̂ł��傤���B�Ƃ����̂́A�C���t���G���U�̖�̃^�~�t���Ƃ��A�������U�Ƃ��A�݂�ȏo�Ă���Ƃ���̌������Ƃ����j�Q���܂���ˁB
�o���F
�����ł��ˁB��قǂ̉f���ɂ�����܂�����ˁB
KK�F
������A����ōs���ƁA���̃E�C���X�ASARS-Cov2�ɑ��ẮA�����̍זE���痣���Ƃ���̂���͂Ȃ��ł���ˁB�e�Ղɗ���邩��A�K�v�Ȃ���ł��傤���B
�o���F
�����ł��ˁB�o�čs���Ƃ���ɑ����͂Ȃ��ł��ˁB����邩����Ȃ����A���������m�������邩�ǂ������͒m��Ȃ��̂ł����A�זE�ɓ�����́Aendocytosis�A�זE����o�čs���Ƃ����exocytosis�ƌ����̂ł����A�זE���痣��Ȃ��̂́A�E�C���X���ʂ̎�������Ă��āA�����ɂ������Ă���̂ł͂Ȃ����Ǝv���܂��B
KK�F
������A�C���t���G���U�E�C���X���C���[�W�����̂ł����A�����̂Ƃ���͂ǂȂ����G��Ă��Ȃ��悤�ŁA�ǂ��Ȃ̂��ȂƎv���Ă��܂����B
�o���F
�����ł���ˁB�����炭�͉����������Ȃ��ŁA�o�čs�������������̂�������܂���ˁB�ł������A�������Ă���Ƃ�����A��������߂�A���邢�͗���Ȃ��悤�ɂ���A������������͌��ʓI��������܂���B
KK�F
�����������J�j�Y��������̂��ȁB�������킩��Ȃ��������̂ł�����B
��c�F
�Ȃ�قǁB
KK�F
�C���t���G���U�E�C���X�̏ꍇ�́A�����̂Ƃ���̖L���������̂ŁA�V�^�R���i�E�C���X�ł������������z�����Ȃ��̂��ȁA�Ǝv������ł����B
�o���F
�����A��������g���Ă���i�K�ł́A�������b�������v���Z�X�Ɍ������Ƃ��킩���Ă���̂ł����A�V����J�����鎞�_�ł́A���������Ƃ�����d�_�I�ɏڂ������ׂĐV���n��K�v������܂���ˁB�f���炵�����_���Ǝv���܂��B
��c�F
�͂��A���肪�Ƃ��������܂��B
KK�F
���A���ł͂Ȃ��̂ł����A�C���t���G���U�E�C���X�ƈ���āA���̃E�C���X��m-RNA�̓V���O����1�{�����Ȃ��āA�ォ����ł���ˁB����ŁA�������^���p�N��������ł����A�ŏ���1�{(�C���t���G���U��8�{�����ł���)�B������ CAP*�̏��͂���̂ł���?
*CAP=m-RNA�̏���ǂ�Ń^���p�N�������(�|��)���ɁA�ŏ��ɓnj��n�߂�|��J�n�̖ڈ�
CAP��}�������͂���̂ŁA������g���A�|��������Ȃ��悤�ɂł���̂ł͂Ȃ����Ǝv�����̂ł����A�ł��V�����E�C���X������A���̕ӂ��܂��킩���Ă��Ȃ��̂�������܂���ˁB
*CAP=m-RNA�̏���ǂ�Ń^���p�N�������(�|��)���ɁA�ŏ��ɓnj��n�߂�|��J�n�̖ڈ�
CAP��}�������͂���̂ŁA������g���A�|��������Ȃ��悤�ɂł���̂ł͂Ȃ����Ǝv�����̂ł����A�ł��V�����E�C���X������A���̕ӂ��܂��킩���Ă��Ȃ��̂�������܂���ˁB
�o���F
������x�A���炩�ɂȂ��Ă���Ǝv���̂ł�����ǂ��E�E

��c�F
�Ȃ�قǁB�C���t���G���U�Ɣ�r�������ɁA�C���t���G���U�E�C���X�Ŋ�������Ă�����Ԃ̃��J�j�Y�����A���̂܂ܓK�p�ł��Ȃ��̂��ȂƂ����^�₩��l����ꂽ��ł��ˁB
�o���F
�����ł���ˁB
KK�F
���ꂱ���A�C���t���G���U�͂悭�킩���Ă���Ǝv���̂ŁB��͂�V�����a�C������A�Ⴄ�̂�������܂��B
�o���F
�V�����o�Ă����E�C���X�ł�����A�܂������ޗ������Ȃ��̂�������܂���ˁB
KK�F
���ƁA�搶�̂��b�ŁA�q�g����q�g�ւ̊����̂��b������܂������A���ɒ����ł̓R�E��������n�܂����Ƃ��A���̓����͂ǂ��Ȃ�ł����B
�o���F
�L�����������Ƃ����b������܂��B�l�Ԃ����ł͂Ȃ���������܂����ˁB
KK�F
���̕ӁA�܂����炩�ł͂Ȃ��̂�������܂���ˁB
��c�F
�C���t���G���U�ƈ���āA�}���ɐ��E���Ɋ����҂��������Ƃ������ƂŁA�����̂������A�����Ƃ���ł���Ă��銴���ɂȂ��Ă���̂�������܂����ˁB���̕Ӓm�肽���Ƃ���ł��ˁB
�o���F
�����ł���{�݂����Ȃ��̂�������܂���B�������L����Ȃ��悤�Ȍ��d�Ȏ������ł��Ȃ��ƁA�������������͂ł��܂����ˁB
��c�F
�Ȃ�قǁB

TT�F
m-RNA���N�`���ɂ��Ăł����A���̎�ʼn������R�������ĖƉu�����œ�������Ƃ����̂͂킩��₷���ł����Am-RNA���N�`���Ƃ����̂́A���ɃX�p�C�N�^���p�N��m-RNA�������Ă��āA����̓E�C���X�Ɠ����悤�ɁA�q�g�̃|�������[�[�ŕ���������Ƃ������ƂȂ̂ł���?
�o���F
�������Ǝv���܂��B�������ׂ������̒��ɂ̓X�p�C�N�^���p�N�Ƃ����\���͂Ȃ�������ł����A�V�^�R���i�E�C���X�������Ă���^���p�N���̈�{��m-RNA�Ƃ����\��������܂����B���������^���p�N����̓��Ŏ��R�����̂悤�ɍ��郏�N�`�����Ɨ������Ă��܂��B�A�X�g���[�l�J�̃��N�`���̕��́A�A�f�m�E�C���X�̒��ɂ��̃X�p�C�N�^���p�N��������悤�Ȉ�`�q��g�ݍ���ł���Ɨ������Ă��܂��B
��c�F
��낵���ł����B
TT�F
���肪�Ƃ��������܂��B
TA�F
���͂�����Ƌ^��Ȃ̂́A�����o�H�ŁA��Ƃ��Ĕ����ƌ����܂����A�ɕY���Ă���}�C�N���A���̋��ЂƂ����̂��ǂꂭ�炢�̂��̂Ȃ̂��B
�o���F
�������C�����ł����B

TA�F
����l�ɂ��A��C�ɕY���Ă���̂́A�����Ȃǂ��A��C�ƈꏏ�ɓ����Ă���̂ŁA�x�̂�艜�܂ōs���Ă��܂��āA���d�lj����₷���Ƃ�����������݂����Ȃ�ł����B
�o���F
�V�^�R���i�E�C���X�̏ꍇ�́A���ꎩ�g����C�̒��ɕY���p�x�͏��Ȃ��悤�ŁA�����Ԃ��ĂΎ��O�����ʼn��Ă��܂��Ƃ���������܂��B�����}�̂�����́A�����Ƃ��A�����������̂��Ȃ��Ƌ�C���ɂ͂Ȃ��ƁA���͗������Ă��܂��B�Ȃ̂ŁA�������Ƃ��Ă����ʂ��Ǝv���܂��B�z�����Ƃ��Ă��A���R�Ɖu���ł��邭�炢�̏��Ȃ��ʂ��ƍl���Ă��܂��B
��c�F
�͂��A��낵���ł����B
MS�F
�R�ۖ�͋ێ��̂�@���܂����A�R���i�E�C���X�̏ꍇ�́A�l�ԑ��̐N����h������A������Ƃ����}������Ƃ�����̂�����������܂������A�E�C���X���̂���������A�E�C���X���̂�j���͂Ȃ��̂ł����B
�o���F
����́A�A���R�[���ł��B
��c�F
�����A�Ȃ�قǁB(���:��)
MS�F
�����Ă݂�A�Ȃ�قǂ����ł��ˁB

�o���F
��ɂ���āA��ɂ������̂͐����B�A���R�[���́A�E�C���X�̃G���x���[�v���A����m-RNA���O�ɏo����Y�^�Y�^�ɔj���̂��Ǝv���܂��B
��c�F
�A���R�[����p���āA�ނ��o���ɂ��������Ƃ������Ƃł��ˁB
�o���F
�͂��A�����ł��B����Ɋ֘A���Ăł����A�t�@�C�U�[��m-RNA���N�`�����}�C�i�X75���ŕۑ����Ȃ��Ă͂����Ȃ��Am-RNA�͊j�_�������ɂȂ������\�������Ă��܂��B���̍��̂Ȃ��ڂ͔��Ɏア�̂ł��B���w�������N����₷���B�퉷�A���邢�͉��x�������Ȃ�ƁA���w�������N����₷���B������A��������邽�߂ɂ��ቷ���ŕۑ����Ȃ��Ă͂Ȃ�Ȃ��B
���ꂩ�玉������Ȃ�i�m�p�[�e�B�N���ŕ��ł��ƁA���艻����悤�ł��B�ŋ߁A�}�C�i�X20���ł������Ƃ�����������܂����B�����A���̃i�m�p�[�e�B�N������`�q������Ă���̂��Ǝv���܂��B
���ꂩ�玉������Ȃ�i�m�p�[�e�B�N���ŕ��ł��ƁA���艻����悤�ł��B�ŋ߁A�}�C�i�X20���ł������Ƃ�����������܂����B�����A���̃i�m�p�[�e�B�N������`�q������Ă���̂��Ǝv���܂��B
MS�F
���ƁA���͂ǂ��ł����B�m���E�C���X�ł�100�ł���������Ƃ��A�R���i�E�C���X�͉����炢�ŕ|���̂ł��傤���B���Ȃ���A���̂ւ�ɂ����Ă����C�ł����B
�o���F
���C���Ǝv���܂��B��قǃ}�X�N�̘b�����܂������A���Ȃ���Α̂̒��ŖƉu���͂��炭�̂ł��B�R�̂��ł���̂ł��B��ʂɓ���̂����ŁA��������H�͐������Ă��������A�Ƃ������Ƃ��Ǝv���܂��B
�@�C�����Ȃ���Ȃ�Ȃ��̂́A���N�`����ł����炻��ł��ׂĊ����Ƃ������Ƃł͂Ȃ��̂ł���ˁB�l�͏��Ȃ��Ƃ����N���炢�͎O����������āA�}�X�N�����Đ�������̂������̂ł͂Ȃ����Ǝv���܂��B�ǂ��ł��傤���B
�@�C�����Ȃ���Ȃ�Ȃ��̂́A���N�`����ł����炻��ł��ׂĊ����Ƃ������Ƃł͂Ȃ��̂ł���ˁB�l�͏��Ȃ��Ƃ����N���炢�͎O����������āA�}�X�N�����Đ�������̂������̂ł͂Ȃ����Ǝv���܂��B�ǂ��ł��傤���B
KK�F
��{�I�Ȏ���ł����A����҂Ƃ���b�����̂�����̕�����Ȃ��Ƃ����̂́A�����P�ɁA�Ɖu�̋@�\�������Ă���Ƃ��A�̗͓I�Ȗ��ł����B
�o���F
������ł��ˁB��͂�A�Ɖu�\���N�ƂƂ��ɗ����Ă���̂���Ԃ̌������Ǝv���܂����A�������q�_�I�Ɍ�������ǂ��Ȃ̂��B�R�̂��Y������זE������ƂƂ��Ɍ`���ς��Ƃ��A���邢�͍זE���̂̐�������Ƃ��B����Ƃ������Ƃ͖�w���̐��̐搶���畷�������Ƃ�����̂ł����A�����������Ƃɂ��W���Ă���Ǝv����ł��B
��c�F
�݂Ȃ���o�Ă���^����Ă��Ă��A�܂��܂��킩��Ȃ����Ƃ���������Ȃ��Ɗ����܂��B���̒��ŋً}���Ԑ錾���o����Ă��܂����A���낢�돤������Ă�������{���ɍ����Ă���������̂ŁA�Ȃ�Ƃ��������N���炢�ł����܂��Ăق����Ȃ��Ǝv���܂��B
�@����Ȓ��ŁA�݂Ȃ���ɂ͍����̂悤�Ȃ��b������ɓ`���Ă��������āA�ӎ������߂āA���ʂ悭�Ȃ�Ƃ��R���i��}���Ă��������Ǝv���܂��B
�@�o���搶�A���肪�Ƃ��������܂����B (����)
�@����Ȓ��ŁA�݂Ȃ���ɂ͍����̂悤�Ȃ��b������ɓ`���Ă��������āA�ӎ������߂āA���ʂ悭�Ȃ�Ƃ��R���i��}���Ă��������Ǝv���܂��B
�@�o���搶�A���肪�Ƃ��������܂����B (����)
�C�x���g���z����������
mail�Fevent@icam.co.jp TEL�F03-6905-6610 / FAX�F03-6905-6396
