戞76夞 擔杮嵶嬠妛夛憤夛
2003擭04寧01擔乮壩乯-03擔乮栘乯丂応強丗儂僥儖擔峲孎杮
擔杮嵶嬠妛嶨帍丂58(1)187, 2003
傾僈儘乕僗僽儘僢僋傪梡偄偨
峈嬠栻栻暔摦懺僔儈儏儗乕僔儑儞偺偨傔偺怴偟偄in vitro幚尡姶愼儌僨儖
晉揷曌1), 媏抮尗2), 怷嶳傂偲傒1), 屗捤嫳堦2)
1) 姅幃夛幮僔僱丒僒僀僄儞僗尋媶強丄2) 搶嫗彈巕堛壢戝妛姶愼惂屼壢
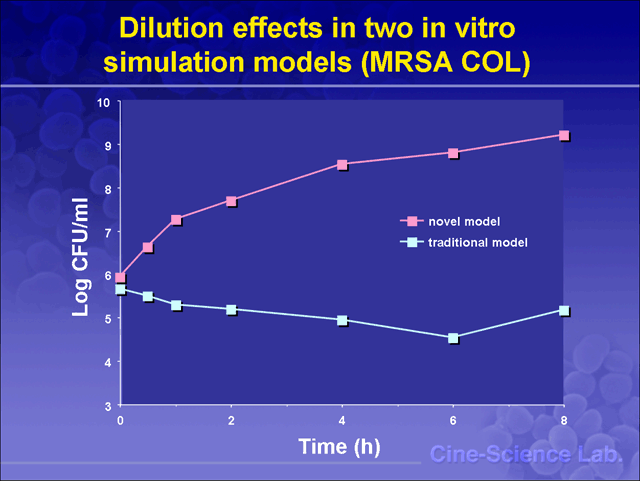
僸僩偺栻暔摦懺傪斀塮偟偨峈嬠栻偺in vitro幚尡姶愼儌僨儖偼in vivo姶愼儌僨儖丄椪彴帯尡偺慜偵丄峈嬠栻偺桳梡惈傪敾掕偡傞忋偱晄壜寚偱偁傞丅偟偐偟丄廬棃偺儌僨儖偼搳梌弶婜偺姶愼昦懺傪斀塮偱偒側偄偱偄偨丅偙偺偨傔丄斀墳憛偵僼傿儖僞乕傪愝抲偡傞側偳偺懳嶔偑庢傜傟偨偑丄栚媗傑傝側偳偺栤戣偺偨傔偵幚梡壔偵偼掱墦偐偭偨丅変乆偼掅梈揰傾僈儘乕僗偵惗嬠傪晻擖偟偨僽儘僢僋偵傛傝丄偙偺栤戣傪崕暈偟偨怴偟偄峈嬠栻栻暔摦懺僔儈儏儗乕僔儑儞偺in vitro幚尡姶愼儌僨儖傪奐敪偟偨丅
懳徾嬠偵偼墿怓僽僪僂媴嬠MRSA COL偲MSSA RN2677傪丄懳徾栻嵻偲偟偰cefazolin,
ampicillin/sulbactum傪梡偄偨丅栻暔摦懺儌僨儖偼one compartment model傪梡偄丄斀墳憛偺嬠塼傪廬棃朄偺僒儞僾儖偲偟偨丅怴朄偼嬠傪1.5%掅梈揰傾僈儘乕僗偵晻擖偟丄僫僀儘儞儊僢僔儏忋偱屌傔丄斀墳憛偵擖傟丄宱帪揑偵嵦庢偟偨丅僽儘僢僋偼丄傾僈儔乕僛1U偱張棟偟丄惗嬠悢應掕傪峴偭偨丅斀墳憛丄傾僈儘乕僗僽儘僢僋撪偺栻暔擹搙傪bioassay朄偵偰妋擣偟偨偲偙傠丄偄偢傟偺應掕帪娫偱傕椉幰偼傎傏堦抳偟偰偄偨丅廬棃朄偱偼栻暔搳梌奐巒偐傜3帪娫偼婓庍岠壥偵傛傝惗嬠悢偑尒偐偗忋憹壛偟偰偙側偐偭偨丅
堦曽丄怴朄偱偼捈屻傛傝懳悢憹怋偑摼傜傟丄惗嬠悢偺尭彮偼尒傜傟側偐偭偨丅MSSA
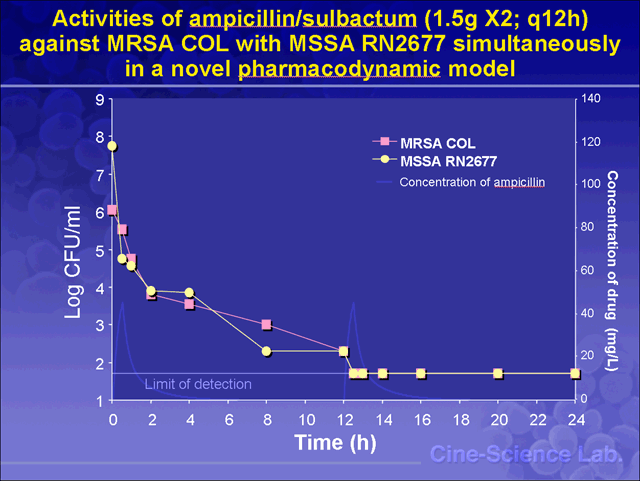
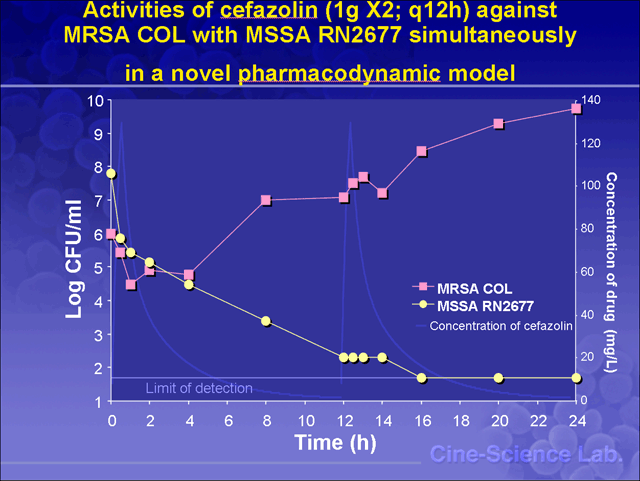
RN2677丄MRSA COL偵懳偟丄ampicillin/sulbactum偱偼1.5g偺1夞側偄偟丄12帪娫偍偒偺2夞搳梌偱彍嬠壜擻偱偁偭偨丅cefazolin偼MSSA偵懳偟偰偼1g1夞搳梌偱偼12帪娫埲崀偵嬠偺嵞憹怋傪擣傔丄彍嬠偵偼2夞搳梌偑昁梫偱偁偭偨丅MRSA
COL偵懳偟偰偼cefazolin偼桳岠側岠壥傪帵偝側偐偭偨丅
偙偺寢壥丄ampicillin/sulbactum偼忢梡検偱傕 MRSA偺帯椕栻偲偟偰巊梡偟偆傞偙偲偑婜懸偝傟偨丅崱夞奐敪偟偨幚尡姶愼儌僨儖偼丄娙曋偱惗懱撪偺栻暔摦懺偲姶愼昦懺傪摨帪偵嵞尰偱偒傞桪傟偨宯偲峫偊傜傟偨丅
亂妛夛敪昞傛傝敳悎丅亃恾偼僋儕僢僋偡傞偲戝偒偔昞帵偝傟傑偡丅
僸僩偺栻暔摦懺傪斀塮偟偨峈嬠栻偺in vitro偺幚尡姶愼儌僨儖偼丄椪彴偱偺峈嬠栻偺桳岠惈傪敾掕偡傞偨傔偵晄壜寚偱偡丅摿偵丄懴惈嬠偺弌尰傪嫋偝側偄搳梌朄側偳丄峈嬠栻偺傛傝桳岠側巊梡朄偺専摙偵寚偐偣傑偣傫丅偟偐偟丄栻嵻擹搙傪婓庍偵傛偭偰曄壔偝偣傞偨傔丄偙傟傑偱偺懡偔偺儌僨儖偼丄偦偺婓庍岠壥偵傛傝丄幚梡忋栤戣偑偁傝傑偟偨丅
崱夞偺栚揑偼婓庍岠壥偵傛傞廬棃朄偺栤戣揰傪夝寛偟丄僔儞僾儖偱怣溸惈偺崅偄in vitro栻暔椡妛幚尡儌僨儖傪奐敪偡傞偙偲丄偝傜偵奐敪偟偨儌僨儖傪梡偄偰丄峈嬠栻偺巊梡偵傛偭偰丄懴惈嬠偺慖戰偑婲偙傞偐偳偆偐傪in
vitro偱専徹偡傞偙偲偱偡丅
廬棃偺曽朄偱偼晜梀忬懺偺嬠傪愙庬偡傞偙偲偵傛傞栤戣揰偑嫇偘傜傟傑偡丅
栻嵻擹搙曄壔傪幚尰偡傞偨傔偺媫懍側婓庍偵傛傝丄宯奜傊偺嵶嬠偺棳弌偑旔偗傜傟傑偣傫丅偙偺偨傔丄寢壥偺夝庍偵偼斚嶨側僨乕僞偺曗惓偑昁梫偵側傝傑偡偑丄惓偟偔曗惓偡傞偙偲偼擄偟偄偲尵傢偞傞傪摼傑偣傫丅
偦偙偱丄崱夞偺幚尡偱偼丄嵶嬠傪姦揤偵杽傔崬傫偱栻嵻傪嶌梡偝偣傞偲偄偆丄怴偨側栻暔椡妛儌僨儖傪峫埬偟傑偟偨丅
嬠悢偺憹尭偼 強掕帪娫偱庢傝弌偟偨姦揤僽儘僢僋偐傜嵶嬠晜梀塼傪摼偰丄暯斅姦揤攟抧偵揾晍偟丄僐儘僯乕悢傪僇僂儞僩偟偰峴偄傑偡丅
晜梀忬懺偺嬠傪栻嵻偵敇偡廬棃朄偱偼丄娏棳偵傛傞婓庍岠壥偵傛傝丄尒偐偗忋嬠偺憹怋偑尒傜傟側偄丅幚嵺偵偼憹怋偟偰偄傞偺偱丄應掕抣偺曗惓偑昁梫偵側傞丅偙傟偵懳偟崱夞偺曽朄偱偼丄懍傗偐側嬠悢偺憹壛偑娤嶡偝傟傑偡丅婓庍偵傛傞塭嬁偼尒傜傟偢丄應掕抣傪曗惓柍偟偵偦偺傑傑埖偆偙偲偑偱偒傑偡丅
MSSA偲MRSA傪100丗1偱崿榓偟偰摨偠姦揤僽儘僢僋偵晻偠丄傾儞僺僔儕儞/僗儖僶僋僞儉傪嶌梡偝偣偨寢壥偱偡丅
12帪娫偍偒2夞偺搳梌偱偼丄偙偺傛偆偵MRSA, MSSA偲傕偵徚幐偟傑偟偨丅
堦曽丄僙僼傽僝儕儞1倗2夞搳梌偱偼丄MSSA偼徚柵偟傑偟偨偑丄彮検崿榓偟偨MRSA偑憹怋偟丄慖戰偝傟傞偙偲偑妋偐傔傜傟傑偟偨丅
崱夞奐敪偟偨怴儌僨儖偺儊儕僢僩偼丄僐儞僩儘乕儖攟梴偱偺嬠悢掅壓偑尒傜傟偢丄應掕抣偺曗惓偑晄梫偱偁傞偙偲丄堦夞偺娏棳幚尡偱娙扨偵暋悢僒儞僾儖偑埖偊傞偙偲丄摨條偵暋悢嬠姶愼偺儌僨儖偲偟偰巊梡偱偒傞偙偲丄偝傜偵丄掕拝偟憹怋偡傞偲偄偆丄惗懱撪偱偺姶愼昦懺偵嬤偄忬嫷傪嵞尰壜擻偱偁傞偲偄偆偙偲偑嫇偘傜傟傑偡丅
傑偨丄僨儊儕僢僩偲偟偰偼嬠悢應掕偺偨傔丄姦揤偐傜嵶嬠晜梀塼傪摼傞偨傔偺張棟夁掱偑嫇偘傜傟傑偡偑丄20暘掱搙偱偁傝丄曗惓偺梫傜側偄怣棅惈偺崅偄僨乕僞傪摼傜傟傞偙偲傪峫偊傞偲昁偢偟傕僨儊儕僢僩偲偼偄偊傑偣傫丅
埲忋丄崱夞偺幚尡傪傑偲傔傑偡偲丄傾僈儘乕僗僽儘僢僋偵嬠傪晻擖偟偨丄怴婯栻暔摦懺椡妛儌僨儖傪奐敪偟傑偟偨丅偙傟偼丄廬棃朄偺栤戣揰傪夝寛偟丄娙曋偱怣棅惈偑崅偔丄偟偐傕埨壙側桪傟偨曽朄偱偡丅懡嵻懴惈嬠姶愼偵懳偡傞帯椕朄傪専摙偡傞忋偱傕丄桳梡側僣乕儖偲惉傝摼傞傕偺偲峫偊傑偡丅
偙偪傜偺僐儞僥儞僣傪偛棙梡偄偨偩偔偵偼AdobeFlashPlayer偑昁梫偱偡丅
昁梫側曽偼Adobe幮偺僒僀僩偐傜僟僂儞儘乕僪偟偰偔偩偝偄丅